神经内分泌肿瘤肝转移1例
2014-09-04 22:04:36 来源:37度医学网 作者: 评论:0 点击:
病例简介
病史
患者男性,41岁。2011年5月,无明显诱因出现左上腹持续性隐痛,约2小时后自行缓解,遂至当地医院。
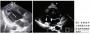
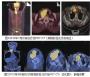
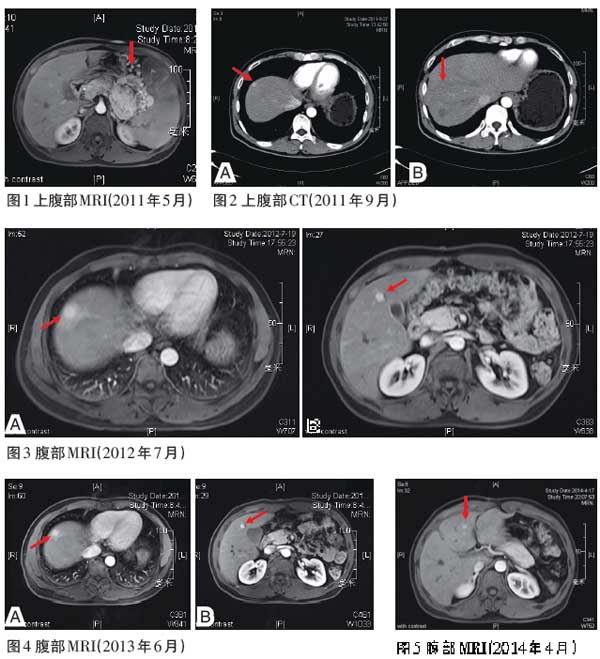
辅助检查上腹部CT提示左侧腹膜后脾肾间隙低密度灶,疑似“副节瘤”。2011年5月,我院B超提示左侧腹部实质占位,疑似腹膜后或胰尾来源恶性肿瘤(MT),侵犯脾脏;上腹部磁共振成像(MRI)(图1)提示左胰脾间隙占位,考虑来源于胰尾部神经内分泌肿瘤(NET)可能大;累及脾静脉伴胃周大量侧支循环。
治疗
2011年5月于我院行胰体尾肿瘤切除术+脾切除术。病理检查提示(胰体尾及脾)NET(G2),核分裂象3~5/10个高倍视野,脉管 内见瘤栓,侵犯脾脏,胰头切缘未见累及;免疫组化(IHC)染色结果,突触素(SYN)(++),嗜铬粒蛋白(CHG)(+),CD56(++),血管活 性肠(VIP)(-),胰多肽(PP)(弱+),神经元胞体(Soma)(+),5羟色胺(5-HT)(-),胃泌激素(gastrin)(+),胰岛素 (insulin)(-),胰高血糖素(glucogan)(+),促肾上腺皮质激素(ACTH)(-),核蛋白Ki67(1%~2 %+),CD10(-),β-链蛋白(β-cat)(部分+),CD99(+/-),E-钙粘附分子(E-cad)(-),细胞角蛋白(CK)(广) (+),波形蛋白(VIM)(-)。术后定期随访未见复发或转移征象。
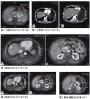
2011年9月腹部CT(图2)示胰腺术后改变,肝脏两枚低密度影;考虑转移性肿瘤。甲胎蛋白(AFP)、癌胚抗原(CEA)及糖类抗原(CA)19-9均(-)。
2011年10月行第1次肝动脉化疗栓塞术(TACE)。造影见肝右叶膈顶可疑片状染色灶,肝右叶下角有0.8cm圆形染色灶,超选至肝 固有动脉,注入5-氟尿嘧啶(5-Fu)1.0g+顺铂(DDP)80mg化疗,超选至肝右动脉,予以丝裂霉素(MMC)10mg+超液化碘油7ml混悬 液栓塞。
2012年7月腹部MRI(图3)示胰腺癌肝转移,肝右叶转移灶与2012年4月相仿(肝右前叶上、下段各见结节灶,最长径分别为1.5cm、1.1cm,右后叶上段结节灶,最长径约1.8cm),异常灌注较前明显。
2012年7月行第2次TACE术。造影见肝右叶两肿瘤染色灶(约1.5cm、2cm),超选至肝右动脉,注入5-FU0.75g+奥沙 利铂100mg化疗,予MMC10mg+超液化碘油4ml混悬液栓塞,病灶碘油沉积。神经元特异烯醇化酶(NSE)18.2ng/ml。
2013年3月腹部MRI示胰腺NET术后,肝转移灶介入术后,肝内病灶较前(2012年11月)相仿。
2013年6月腹部MRI(图4)示为胰腺NET术后及肝转移介入后,肝内病灶异常强化。
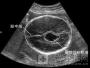
2013年7月肝脏超声造影提示肝右后叶实质占位,考虑血管瘤;肝右前叶膈顶部胆囊旁实质占位,考虑MT可能,介入治疗后改变;肝右前叶胆囊上方实质占位,考虑血管瘤;肝脂肪浸润;肝囊肿。
2013年7月行特殊肝段切除(肝右叶部分切除,切缘0.5cm)+胆囊切除术。术中B超定位肿瘤2枚,分别位于右前叶膈顶部(直径约 2.5cm×2cm×2cm,界清,无包膜)及肝右叶临近胆囊(直径约1cm);肝门淋巴结无肿大,门脉主干及左、右分支无癌栓。病理检查示(肝右 叶)NET(G2)。
复习胰体尾手术病理切片,两者形态基本相似,故考虑本次肿瘤为胰腺NET肝转移(2枚),(胆囊)慢性炎。IHC染色示AFP(-),肝 细胞(Hepa)(-),CD34(血管丰 富),CK19(++),CK7(-),Ki67(15%+),CHG(+),SYN(++),CD56(++),VIM(-),CD10(+),抗抗胰 蛋白酶(a-AT)(++),抗糜蛋白酶(a-ACT)(-)。
2014年4月腹部MRI(图5)示肝MT转移介入及术后病例,肝近膈顶病灶与2013年6月相仿,肝左内叶两枚小新发灶可能。B超引导下肝肿瘤射频消融(RFA)毁损术(针对左内叶11mm×8mm占位)。
患者病程中无面色潮红、出汗、腹泻、腹部绞痛、支气管痉挛、水肿、消化道出血等症状;目前一般情况可,近期有糖耐量异常。
肿瘤内科讨论
胃肠胰腺神经内分泌肿瘤(GET-NET)是一组起源于肽能神经元和神经内分泌细胞的异质性肿瘤,原发灶最常见于胃黏膜、小肠和大肠、直 肠或胰腺。根据肿瘤是否具有激素分泌功能和有无出现激素引起的临床症状分为非功能性和功能性肿瘤,大部分GET-NET为非功能性,功能性NET居多。
2014版美国国立综合癌症网络(NCCN)根据核分裂象和Ki67指数将NET分G1、G2和G3级别,研究显示Ki67与患者生存率强相关(尤其是胰腺NET),且可作为胰腺损伤预后因子。
通常认为,NET非常罕见,但实际发生率正在逐年增长(3.65/100000/年),大部分NET生长缓慢,难以早期发现,通常 65%~95%的病例在诊断时已发生转移,肝脏和淋巴结是最常见的转移部位。不论NET原发部位在哪里,肝转移是最关键的影响预后的因素,回顾性研究显示 肝转移患者的5年总生存(OS)率为13%~54%,未发生肝转移的患者5年OS率为75%~99%。肠道NET发生转移的病例5年OS率为 56%~83%,胰腺NET发生转移的5年OS率为40%~60%。
尽管目前NET肝转移的治疗手段复杂多样,手术切除仍是唯一可能根治的方法。对于不能切除的病灶,选择最佳的治疗时机和治疗方案对于改善 患者的生活质量和延长OS期至关重要。内科治疗主要为药物治疗,包括常用的化疗方案(链脲霉素+5-Fu/多柔比星;依托泊苷+顺铂)、生长抑素类似物、 mTOR抑制剂、多靶点酪氨酸激酶抑制剂(TKI)。
对于无症状胰腺NET(pNET)的内科治疗模式。欧洲肿瘤内科学会(ESMO)的建议为,任何部位转移性NET(G2)和神经内分泌癌 (NEC)(G3)推荐化疗;化疗用于NET(G1)反应率很低,<15%(Ⅲ,A)。无法手术的进展期pNET肝转移患者(G1/G2),可使用 系统性细胞毒药物,如脲链霉素+5-Fu/多柔比星,客观缓解率为35%~40%(Ⅱ,B);以替莫唑胺为基础用药的化疗(单药或联合卡培他滨)治疗 pNET,部分缓解率较高(40%~70%)(Ⅲ,B);NEC(G3)伴肝转移,无论原发部位,推荐早期使用化疗药物顺铂/依托泊苷。
分化差的NET目前无标准二线治疗方案,可单用替莫唑胺或与卡培他滨±贝伐珠单抗(Ⅲ,B)。5-Fu或卡培他滨联合奥沙利铂或伊立替康等方案也可以作为二线治疗的选择。
肝肿瘤外科讨论
外科手术治疗在缓解难治性神经内分泌症状及为患者提供进一步治愈机会上均有不可替代的作用。肝转移是影响胰腺神经内分泌肿瘤(pNET) 患者生活质量和长期生存的主要因素,应采取以外科治疗为核心的多学科协作(MDT)治疗,主张一次或多次尽可能切净原发灶与转移灶。pNET肝转移常表现 为双叶多发病变,肿瘤负荷高,将MDT与传统手术相结合,不但可成为有效的姑息治疗手段,还可能使部分转移性pNET患者获得治愈机会,最佳的治疗应是针 对患者肿瘤生物学行为的个体化治疗。外科治疗包括根治性部分肝切除、姑息性部分肝切除以及全肝切除肝移植等。
根治性肝切除术唯一具有潜在治愈机会的治疗手段,但适应证仅约10%~20%[病理分级低(G1、G2)、转移灶单一或能一次切除;综合 治疗后二期肝切除术可完全(R0)切除者]。多数病例会在5年内复发,部位仍以肝脏为主,患者的5年总生存(OS)率达40%~80%。
姑息性肝切除术或称减瘤手术适应证人群为20%~25%[非手术疗法(局部消融或介入治疗)无法缓解或治疗失败的神经内分泌症状]。为确 保术后症状缓解,预计切除肿瘤容积应≥总体肿瘤负荷的90%,治疗效果良好,90%的患者可在2年内满意地控制症状,并有可能适当改善长期生存。转移性 NET经常合并难治性神经内分泌症状,80%患者不具备根治性切除可能,此时,姑息性肝切除在改善患者症状及长期生存方面均优于其他非手术治疗手段。
此外,姑息性肝切除还应考虑患者一般状况,充分进行术前准备,以避免术中类癌危象发生。近95%的患者术后可完全改善或部分缓解症状,中 位无症状生存时间达45个月。有研究显示,姑息性肝切除与介入治疗患者的总体症状缓解率相似(92%和91%),无症状生存时间分别为35个月和22个 月,前者明显优于后者(P<0.001)。
肝移植肝移植为有望根治治疗的方法,但其适应证仍充满争议,目前认为,肝移植仅适用于少部分经过严格筛选的患者:①内分泌肿瘤肝脏转移, 无肝外及区域淋巴结转移;②胰腺和原发病灶可完整切除,肝脏双侧叶不可切除的多发转移灶;③Ki67<10%(Ki67<5%预后更好);④ 存在药物无法控制、明显影响患者生命质量的症状,无其他肝移植禁忌证(肝移植禁忌证包括,肝外转移、G3肿瘤、伴发其他恶性肿瘤)。肝移植长期存活率差异 较大,5年OS率为33%~90%,5年无病生存率8%~77%,大部分研究低于30%。由于肝移植资源稀少,筛选患者指征要严格,准确评估、选择合适病 例是保证疗效的关键。
因此,应综合考虑原发瘤切除可能性、转移灶数量及分布、转移瘤负荷、神经内分泌症状及有无肝外转移等因素选择手术方式。肝切除及肝移植均 会在术后面临肿瘤复发风险,采用规律随访策略可及时发现复发病灶并及时处理。随访建议为术后2年内保证每年随访4次,2年后可酌情延长随访周期。
中国胃肠胰神经内分泌肿瘤专家共识
肝切除手术如果手术可达到几乎无肿瘤残余(切除>90%的病灶),可考虑行原发灶和肝转移灶同期或分期切除。手术以尽量达到完全 (R0)或R1切除(显微镜下见癌细胞)为目的,至少应满足以下条件:①分化好的G1/G2肿瘤;②无腹腔外转移及弥漫性腹膜转移;③无右心功能不全;④ 奥曲肽扫描阳性(存在生长抑素受体)者可在减瘤术后给予肽受体放射性同位素治疗。
肝移植年轻患者、肿瘤原发灶已切除、同时不伴肝外转移、分化好的NET(G1/G2),当其他手段难以控制临床症状时,肝移植可作为一种治疗选择。
原发灶和转移灶同期或分期切除及先后分期切除问题
同期切除还是分期切除多数患者采用分期手术。同期手术会增加手术的难度和创伤,但是分期手术的并发症如肝脓肿的发生高于同期。切除 pNET原发病变手术难度及术后并发症发生率均明显高于胃肠道肿瘤。胰瘘、感染、出血均为难以处理的棘手并发症,特别对于无功能性和呈局部浸润性生长的 pNET,确诊时肿瘤体积往往较大,可累及上腹部多个脏器,部分病例需要行风险较高的上腹部脏器切除术才能获得根治。因此,同时性肝转移病变手术决策所面 临的困境是一期同时处理原发病灶和肝转移灶势必明显增加手术难度、创伤和相关术后并发症。
那么,分期手术是否更为理想?美国约翰斯●霍普金斯大学及梅奥诊所的研究者结合两中心数据对应用于胰十二指肠切除术基础上的同期或二期部 分肝切除、局部消融、TACE等治疗策略的围手术期安全性和长期效果进行了系统评价,结果显示,多学科治疗的总体并发症发生率为34.1%,病死率为 2.4%,其中肝脓肿是主要并发症之一,二期较一期治疗的肝脓肿发生率(14.5%对7.0%)更高。这一研究提示,在采用多学科综合治疗处理转移性 pNET时,无论一期处理或分期处理,均应充分考虑相关并发症的预防和治疗。
切除先后有时可先切除转移灶,再切除
上一篇:反复浮肿蛋白尿伴腹胀痛便血
下一篇:病例分享:儿童气管内异物取出新方法
频道总排行
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(12)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)