多发性骨髓瘤治疗目标的争论
2012-03-06 12:31:19 来源:医学论坛网 作者: 评论:0 点击:
争论1:在新治疗时代如何认识CR?
■ 背景
资料表明,无论采用传统化疗、AHSCT或新药治疗,MM患者获得CR或至少≥VGPR的治疗反应与其长期疗效,包括无进展生存(PFS)和(或)总生存(OS),密切相关。
但是,对于MM的治疗目标,我们是否均应尽可能追求获得CR,从而转化为延长PFS和(或)OS?获得CR是否是治疗的终点?回答这些问题,我们需要认识目前CR的定义以及CR与长期疗效的相关性。
CR的定义
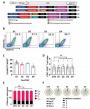
目前,MM患者CR的定义是单克隆蛋白免疫固定电泳检测阴性以及骨髓中浆细胞比例<5%。但这一定义远不能反映疾病控制的最佳状态。采用严格 CR(sCR,血清游离轻链比值正常和免疫组化无克隆型浆细胞)标准已证实,多数CR的患者存在残留瘤细胞。多参数流式细胞和反转录聚合酶链式反应检测证 实的缓解分别为免疫表型和分子生物学缓解。已有研究显示,符合这两种缓解标准的患者可获得更佳的长期疗效。由于MM有骨髓不均一侵犯和髓外侵犯的特性,影 像学检查如磁共振成像(MRI)和正电子发射断层扫描(PET-CT)能更好反映全身性缓解状况,也被证实与预后相关。
CR与长期疗效的相关性
治疗反应深度是MM长期疗效的重要预测因素。
传统治疗时代,仅有<5%的患者获得CR。在这些患者中,治疗反应深度明显提高,并显示出CR与生存相关的优势,转化为延长的PFS和OS。然而在新的治疗时代,多数患者能够获得CR的治疗反应,但这一疗效判断标准已不能高度特异性地反映治疗反应深度。
美国阿肯色大学各阶段TT(Total Therapy)研究的结果显示,患者取得CR是进一步获得长期生存的关键步骤,但并非足够,特别是对 高危患者。尽管高危患者同样可获得高CR率,但易短期内复发并耐药。只有获得持续CR超过3年的患者,OS明显优于未获得CR以及获得CR后3年内复发/ 进展的患者。
因此,MM患者治疗获得CR可能仅反映肿瘤负荷一定程度的消减,而并非完全清除瘤细胞克隆,因而难以预测长期生存甚至治愈。
CR与疾病生物学特性
CR或治疗反应深度在一定程度上反映疾病生物学。美国阿肯色大学前期的TT研究表明,获得CR对长期生存获益的预测仅仅限于基因表达谱 (GEP)检测高危的患者,而对于约85%比例的低危患者,CR与生存无明显的相关性。特别是之前存在意义未明的单克隆丙种球蛋白病(MGUS)表现和 GEP检测为MGUS样基因的患者,即使接受强烈的治疗方案也难以获得CR;同时,研究并未显示此类患者获得CR与提高生存相关。
■ 观点
并非在所有MM患者中,CR均与生存相关。CR与疗效相关性的争议性体现了该标准的不足和局限性。
争论2:控制还是治愈?
■ 背景
基于MM疾病的异质性,许多学者将MM类比于淋巴瘤模式。低危的MM类似于惰性淋巴瘤,现今的治疗难以完全清除瘤细胞克隆而不可治愈,但疾病可 以长期控制;而中危和高危MM则类似于侵袭性和高度侵袭性淋巴瘤,对于治疗更加敏感而存在治愈的可能性。由此进一步引发对MM治疗目的新的争论:控制还是 治愈?对治疗目的的争论同时影响着治疗策略和强度的选择。
MM治疗现状
相比较十余年前,MM的疗效有了显著提高,新药治疗时代的中位生存时间在老年和年轻患者分别达到了4~6年和8~10年。
研究初步显示,硼替佐米等新药有可能克服许多传统不良预后因素,如肾功能损伤、高β2微球蛋白水平、13q-和t(4;14)等。但是,大多数 患者仍会经历多次复发而最终耐药,尚难以达到维持慢性状态的真正“长期控制”。而沙利度胺、硼替佐米、来那度胺等新药的长期巩固/维持或再治疗也明显地增 加了毒副作用,影响患者生存质量(QoL)。同时,对于真正高危患者,目前治疗虽明显提高治疗反应和CR率,但易短期内复发并耐药,难以获得长期生存。
MM仍然被认为是不可“治愈”的疾病。首先报道的有可能治愈MM的方法是异基因造血干细胞移植(Allo-HSCT)。不同于多数其他类型的血 液系统肿瘤,MM中位发病年龄超过60岁,因而传统清髓性预处理方案后的移植相关死亡率(TRM)高达约40%,严重限制了其应用,且多个研究的长期随访 仍未显示出生存平台。减低剂量预处理(RIC) /非清髓性移植(NMT)已取代经典清髓性Allo-HSCT,使MM这一中老年疾病的TRM明显降低, 但因复发率增高,PFS和OS并未见明显改善。
传统化疗后AHSCT治疗有3%~10%的患者超过10年仍然保持CR,被认为“临床治愈”。然而,目前这一疗效仅限于很少的患者群体。
基于生物学特性的治疗策略
针对于MM存在的两种生物学特征和治疗现状,以美国梅奥医院(Mayo Clinic)为代表的许多研究组织提出了分层治疗的策略。分层治疗一方面依据年龄和合并症,另一方面根据危险度分层。
分层治疗将低危患者看作惰性疾病难以“治愈”。由于其对每一种治疗均能维持较长的治疗反应期,临床治疗目标可能并不必要获得CR,而选择应用多种方案、序贯治疗使之得到长期、有效“控制”,同时减少毒性和治疗费用。
对于高危、侵袭性表现的MM患者,年轻、合适者应接受强烈的、白血病样的治疗策略,联合多种、有效的治疗药物和方案,尽早达到CR,随后给予强 烈的巩固治疗策略(可包含HSCT),以及长期维持治疗。理论上,其目的是尽可能地消除瘤细胞克隆,尽快获得并维持最佳治疗反应,避免残留肿瘤细胞逃逸或 获得继发细胞遗传学异常从而产生耐药。
目前该治疗策略的有效性尚未被完全证实,随着新药的开发,这一模式可能随之改变。同时,类似于淋巴瘤,即使我们通过这种模式能够治愈高危患者,也不能盲目推广至低危、惰性的患者,这可能增加毒副作用而没有提高疗效。
然而,我们对分层治疗和治疗目标的认识是存在时限性的,随着新药治疗的进展,这一认识会随之改变。如近期意大利GIMEMA研究和美国阿肯色大 学TT3研究的结果显示,采用强烈的策略治疗GEP低危的年轻患者,预期持续4年CR的比例为89%,而“治愈”率预计可达50%,显示其可“治愈”潜 能。若长期随访证实该结果,对于年轻低危患者的治疗目标和策略将重新评价。
未来研究方向
总之,以上争论的问题尚远无结论,而针对这些问题的研究将进一步促进对疾病生物学特性的理解以及MM治疗的不断进展。在未来的研究中,我们需要关注以下问题(下表)。
1 深入的基因/遗传学研究,以判断CR是否具有亚型分组或危险度分层的特异性,识别药物敏感和耐药个体, 指导临床研究设计。
2 发展更加敏感、有效的方法和手段评价治疗反应,以避免治疗不足或过度治疗。
3 深入发病和病理机制研究,指导新药和治疗手段的研发。
4 关注临床试验设计,有效平衡疗效和毒性,不断验证和完善分层治疗策略。
上一篇:Allo-HSCT治疗多发性骨髓瘤
下一篇:危险分层及个体化治疗策略
频道总排行
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(12)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)