新发和耐药呼吸道感染新药研发与治疗
2014-12-14 00:20:45 来源: 作者: 评论:0 点击:
2014年11月,Lancet Infect Dis上发表了“新出现的呼吸道感染”系列文章,共5篇,其中第5篇主要描述了呼吸道感染常见和新出现的多种病毒、细菌和真菌病原体,以及针对这些病原体开发和研究的新型抗微生物药物、免疫治疗和宿主导向治疗。现将内容编译如下。
新的和难治性的呼吸道细菌、病毒和真菌病原体可能引起广泛传播,因而成为全球的重大忧患。随着耐药的增加,治疗方法变得局限。然而,具有导致重度呼吸道疾病和广泛传播潜力的新型病毒感染引发了全球的关注。人们已经注意到多药耐药肺结核患者和泛耐药菌的数量显著增加。
随着免疫抑制剂、广谱抗生素和抗肿瘤药的使用越来越多,加上唑类药物的耐药,使得侵袭性肺部真菌感染的数量不断增加,发病率和死亡率居高不下。为了使所有医疗护理机构的呼吸道感染患者获得治疗成功,需要合适、有效及病原体特异性的药物或其他治疗方法。
一、病毒性呼吸道感染
重度急性呼吸综合征冠状病毒(SARS-CoV)的暴发感染、禽流感病毒H5N1的再次出现、奥司他韦耐药的季节性甲型流感病毒H1N1在全球的传播及流行性甲型流感H1N1病毒株pdm09(仍在持续传播)的出现,凸显了当前针对重度呼吸道病毒感染的抗病毒治疗的局限性。
禽流感病毒H7N9的大流行、禽流感病毒H10N8的散发感染、中东呼吸综合征冠状病毒(MERS-CoV)感染的持续暴发及常见呼吸道病毒(如季节性流感病毒、呼吸道合胞病毒、鼻病毒和腺病毒)数量的增加,使得开发更有效的治疗方法以降低发病率和死亡率迫在眉睫。研究的重点是重新开发现有抗病毒药物的一般或特殊用法,以及联合其他辅助治疗,如免疫调节剂和宿主导向治疗。
二、流感病毒
1. 药物
在大多数国家,有两类抗病毒药物获批用于流感的预防和治疗:M2抑制剂(金刚烷胺和金刚乙胺 )和神经氨酸酶抑制剂(奥司他韦、帕拉米韦、扎那米韦和那尼纳米韦;表1)。
表1. 已获批或处于临床开发后期的抗流感病毒药物



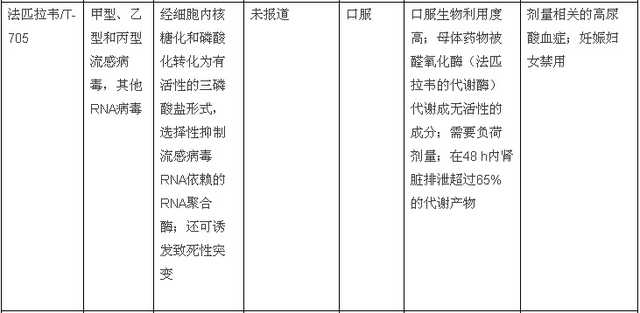
一般来说,对于确诊或疑似的重症、有并发症或进行性加重或入院接受治疗的流感患者,以及有较高流感并发症风险的门诊患者,应尽早开始抗病毒治疗。从出现症状到开始治疗的时间、疾病严重度和病毒复制程度是治疗疗效的关键因素。不能因为诊断而延误治疗。
M2抑制剂(也被称为金刚烷)对乙型流感病毒、近期传播的甲型流感病毒H3N2和2009流行性甲型流感H1N1病毒无效,因这些病毒存在M2离子通道的S31N突变。然而,一部分禽流感H5N1病毒株对M2抑制剂敏感,并且联合使用金刚烷和神经氨酸酶抑制剂可以提高对敏感病毒株的抗病毒活性。
在大多数国家,有两种神经氨酸酶抑制剂被批准使用:奥司他韦和扎那米韦。那尼纳米韦仅在日本获批,帕拉米韦在中国、日本和南朝鲜获批。多项观察性研究显示,住院的重症流感成人患者接受奥司他韦治疗后,死亡率下降,临床预后改善,特别是当症状出现后2天内开始治疗的情况下(当治疗延迟至症状出现后4-5天开始时,可以观察到积极的影响)。
在甲型流感病毒H5N1感染患者出现呼吸衰竭前给予奥司他韦治疗可以降低死亡率,当治疗延迟至症状出现后6-8天开始时,患者可能有获益。住院的重症甲型流感病毒H7N9感染患者接受奥司他韦治疗后,病毒载量下降,预后改善,如病毒因携带Arg292Lys突变而对神经氨酸酶抑制剂出现耐药,则奥司他韦和帕拉米韦的疗效较差,患者预后不良。
奥司他韦的标准治疗疗程为5天;有呼吸衰竭的危重症患者即便接受治疗,其下呼吸道中常存在病毒持续复制,因此建议延长疗程。对于这些患者,增加药物剂量是否能获得更好的抗病毒效果仍在研究中。一项对住院患者(76%为儿童)的随机对照研究显示,给予双倍剂量的奥司他韦相较于标准剂量并无病毒学或临床优势。
虽然住院的乙型流感成人患者接受高剂量奥司他韦治疗后可出现更快的病毒学应答,但在甲型流感患者中并未观察到额外的获益。然而,在一项纳入18例重症2009流行性甲型H1N1流感患者的随机对照研究中,3倍剂量的奥司他韦治疗5天与标准治疗相比可获得显著更高的病毒清除率(78% vs 11%)。正在进行的有关静脉注射神经氨酸酶抑制剂的研究应该能够提供高剂量治疗价值的进一步数据。
扎那米韦和那尼纳米韦的药物敏感性相似。例如,His275Tyr突变导致含N1的病毒对奥司他韦高水平耐药,对帕拉米韦敏感性降低,但不会显著降低对扎那米韦和那尼纳米韦的敏感性。吸入扎那米韦尚未在重症患者中详细研究过,因为在这些患者中,药物能否被有效输送至病毒复制部位及耐受性均未明确。
相比而言,自2009年H1N1流感大流行以来,静脉注射扎那米韦已作为同情性用药而广泛使用,特别是重症H1N1流感成人患者的晚期治疗,以及疑似或明确有奥司他韦耐药的患者。一项研究显示,在安全性评估方面无药物相关趋势,93例基线流感病毒阳性的患者接受2天的治疗后,鼻咽部病毒RNA载量下降的中位值为1.42 log10拷贝/mL。一项针对住院患者的3期研究正在进行中(NCT01014988)。
一项有关吸入那尼纳米韦用于单纯流感的2期随机对照研究显示,在疾病缓解(主要终点)方面并不优于安慰剂。研究纳入了639例患者,评估了40mg和80mg的吸入剂量。流感症状缓解的中位时间在40mg组为102.3小时,在80mg组为103.2小时,安慰剂组为104.1小时(NCT01793883)。
DAS181具有宿主导向的受体破坏作用,从而能够抑制副流感病毒和流感病毒,包括那些对金刚烷胺和神经氨酸酶抑制剂耐药的病毒。在由H5N1和H7N9病毒(包括对神经氨酸酶抑制剂耐药的Arg292Lys突变病毒株)所致的致命性流感动物模型中,外用DAS181有效。
在一项2期随机对照研究中,吸入DAS181可以减少单纯流感患者咽部的病毒复制,但不能降低鼻部的病毒载量或改善临床预后、病例报告显示,吸入或雾化吸入DAS181对免疫功能低下的重症副流感病毒肺部疾病患者可能有效。
法匹拉韦(T-705;6-氟-3-羟-2-吡嗪酰胺)对甲型、乙型和丙型流感病毒有活性,包括对已获批的抗病毒药物耐药的病毒株,并且在较高浓度下,对其他RNA病毒也有广泛活性。法匹拉韦与神经氨酸酶抑制剂联合应用在临床前模型中显示出叠加和协同的作用,但到目前为止临床研究仅局限于单纯流感。
尚未发表的临床研究包括:金刚烷胺、利巴韦林和奥司他韦联合治疗 vs 奥司他韦单一治疗(NCT01227969);硝唑尼特 vs 奥司他韦 vs 联合治疗 vs 安慰剂(NCT01610245);在门诊患者中比较法匹拉韦和安慰剂的随机对照研究(NCT02008344, NCT2026349)。
这些研究显示法匹拉韦的抗病毒效果与奥司他韦相似。一项随机对照研究显示,与安慰剂相比,法匹拉韦可缩短流感症状缓解时间约15小时,进一步的研究正在进行中。
硝唑尼特是一种抗寄生虫药物,且具有免疫调节作用,包括上调干扰素和各种干扰素诱导的基因,以及通过阻断血凝素成熟发挥特定的流感病毒抑制作用。硝唑尼特可在体外抑制流感病毒复制,一项2期随机对照研究显示,对单纯流感具有显著的抗病毒作用(鼻部病毒载量减少1.0 log10),并导致疾病缓解时间明显加快(与安慰剂相差的中位值约20小时)。
一项比较硝唑尼特和奥司他韦及两药联合治疗单纯流感的安慰剂对照研究以及一项在医院中评估其治疗重度呼吸道疾病的研究正在进行中(NCT01610245)。
2. 流感的免疫治疗
非随机研究和病例报告显示,加用含中和抗体的恢复期血浆对SARS患者和重症流感病毒性肺炎(包括由甲型流感病毒H5N1所致的)患者有效。近期一项对现有的采用恢复期血浆或血清治疗SARS和流感研究的系统综述发现,在总体死亡率方面有显著获益。
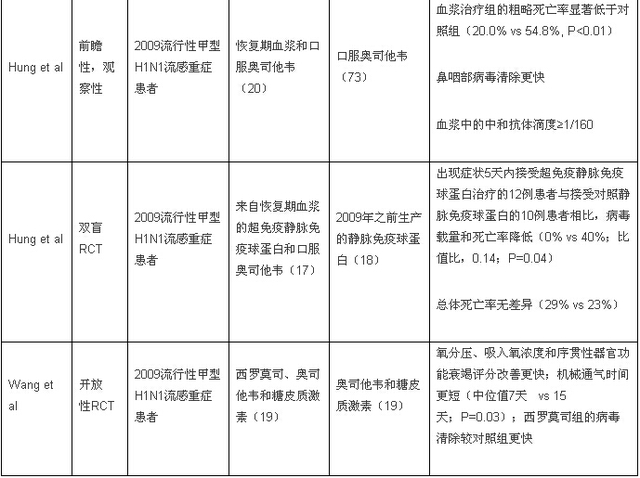
一项前瞻性观察研究显示,重症2009甲型H1N1流感住院患者经血浆治疗后,粗略死亡率下降,鼻咽部病毒清除加快,而一项随机对照研究报道,症状出现5天内给予超免疫球蛋白可使重症疾病的死亡率下降(表2)。在动物实验中非常有效的异型血凝素中和抗体正进入临床评估阶段。
表2. 流感联合治疗临床有效性的代表性研究

3. 抗病毒药物联合治疗
不同作用机制的抗病毒药物(例如,神经氨酸酶抑制剂联合聚合酶抑制剂如法匹拉韦、广谱抗血凝素中和抗体或硝唑尼特)联合治疗重症流感或免疫功能低下患者的感染正在研究中。目前已经在临床前研究中评估了联合使用各种抗病毒药物在提高抗病毒能力、降低耐药率和减少药物剂量方面的作用。然而,关注联合治疗有效性的研究很少(表2)。
相较于不同作用机制的药物联合,采用作用机制相似且剂量最优的药物联合(如双重神经氨酸酶抑制剂)不会提高抗病毒活性,有时甚至产生拮抗。由金刚烷胺、利巴韦林和奥司他韦组成的三联抗病毒方案对甲型流感病毒具有协同的体外抗病毒活性,包括对3种药物均敏感的病毒株,以及对金刚烷胺或奥司他韦耐药的病毒株(包括2009流行性甲型流感病毒H1N1)。
在一项对重症成人患者的回顾性研究中,三联抗病毒药物治疗组和奥司他韦单药治疗组的死亡率无差异,一项由美国国家过敏与感染性疾病研究院发起的针对高风险门诊患者的随机对照研究正在进行中(NCT01227969)。
4. 抗病毒药物联合宿主导向治疗
宿主导向治疗旨在减轻由宿主对病原体的免疫反应所造成的损伤。抗病毒药物联合宿主导向治疗(如免疫调节剂西罗莫司,一种阻断病毒复制所需途径的mTOR抑制剂)也可能提高抗病毒活性。其他可能成为未来临床试验研究重点的宿主导向治疗包括抑制病毒复制所需的细胞靶点(如Raf-MEK-ERK促有丝分裂激酶级联反应和IKK-NF-κB构件)。
辅助性免疫调节治疗在重症流感和其他呼吸道病毒感染中的作用仍不清楚。多项观察性研究显示,2009流行性甲型H1N1流感相关的病毒性肺炎采用全身性糖皮质激素治疗可导致发病(如继发感染)和死亡风险增加,特别是在有效的抗病毒治疗延迟或缺失的情况下。使用激素可能延迟病毒清除,并增加耐药和真菌感染的发生风险。
其他潜在的辅助治疗包括静脉免疫球蛋白、N乙酰半胱氨酸、他汀类、大环内酯类、过氧化物酶体增殖剂激活的受体拮抗剂、塞来昔布、美沙拉嗪、血浆净化和血液灌流。在一个动物模型中,氯喹能有效对抗甲型流感病毒H5N1感染,但在其他动物模型和一项人类随机对照研究中则显示无效。
三、MERS-CoV感染
1. 干扰素
MERS-CoV感染可导致重症呼吸系统疾病,有内科合并症的患者死亡率较高。尽管已经对由MERS-CoV和SARS-CoV所致的重度呼吸道感染尝试了多种抗病毒药物经验性治疗,但尚无一种方案在临床试验中接受过严格的评估。在细胞培养和体内,MERS-CoV可削弱天然免疫反应,并延迟促炎细胞因子的诱导产生。这一作用很容易被1型干扰素所抑制(α干扰素,特别是β干扰素),提示干扰素有潜在的治疗价值。
在一个灵长类动物SARS模型中,早期采用聚乙二醇化干扰素α治疗有效,并且在一项SARS患者的非对照研究中,与单独使用全身性糖皮质激素相比,α干扰素联合全身性糖皮质激素治疗可提高氧饱和度,加快影像学上肺部阴影的消退。似乎有理由进一步研究干扰素在MERS-CoV感染中的作用。
2. 抗病毒药物
利巴韦林广泛用于SARS患者,但无任何获益,许多病例可并发溶血性贫血和代谢紊乱。在诱发恒河猴MERS-CoV感染8小时内给予干扰素α2b和利巴韦林联合治疗可减轻肺损伤,适度减少病毒复制(肺部滴度下降<1.0 log10)。多名重症MERS感染患者接受了联合治疗,但感染最终为致命性的,可能的原因是给药时机较晚,处于疾病晚期
。利巴韦林对MERS-CoV有体外抑制作用。利巴韦林对MERS-CoV的抑制浓度非常高,超越了常规剂量方案所能达到的,但大剂量静脉给药可能达到峰浓度。
采用蛋白酶抑制剂洛匹那韦和利托那韦作为SARS的初始治疗与一个匹配的历史队列中使用的利巴韦林单一治疗相比,死亡率(2.3% vs 15.6%)和插管患者比例(0% vs 11.0%, P<0.05)显著降低(洛匹那韦组和利托那韦组:n=44;匹配的历史队列:n=634)。
然而,一项研究报道,奈非那韦和洛匹那韦在体外对抗MERS-CoV的半数有效浓度(EC50)很高,而另一项研究发现,洛匹那韦在临床可达到的浓度下具有抑制作用。
3. 免疫调节和免疫治疗
在细胞培养中,多个药物显示出对MERS-CoV的抑制作用,包括干扰素、环孢素和霉酚酸。霉酚酸在临床可达到的浓度下具有抑制作用,霉酚酸与干扰素β1b联合可使每一种药物的EC50下降1-3倍。二肽基肽酶4(DPP4)也被称为CD26,是MERS-CoV的一种功能性受体,抗CD26的单克隆抗体对MERS-CoV具有体外抑制作用。相比之下,DPP4的酶作用抑制剂(如gliptins)不能抑制病毒复制。
及时给予中和抗体获得治疗成功的几率很高。在发病2周内给予含高浓度中和抗体的恢复期血浆(来自SARS-CoV感染痊愈的患者)治疗相较于发病14天后开始治疗,22天出院的患者比例更高(58% vs 16%)。一些存活的MERS-CoV感染患者有高浓度的中和抗体,如能获得其恢复期血浆,对于其他重症患者可能是一个很好的治疗手段。
全身性糖皮质激素常被经验性用于SARS和MERS-CoV感染以减轻宿主的免疫病理反应。然而,是否有生存获益仍不清楚,一项在香港完成的随机对照研究显示,全身性糖皮质激素可延迟SARS患者的病毒清除。一项回顾性分析显示,SARS患者接受全身性糖皮质激素治疗后预后变差。因此,在前瞻性对照研究证实激素与抗病毒药物联合应用的有效性前,应避免使用激素。
多项观察性研究显示,2009流行性甲型H1N1流感相关的病毒性肺炎或急性呼吸窘迫综合征采用全身性糖皮质激素治疗可导致发病(如继发细菌或真菌感染)和死亡风险增加,特别是在有效抗病毒治疗延迟或缺失的情况下。在需要体外膜氧合治疗的重症甲型流感病毒H7N9感染患者中使用全身性糖皮质激素,可能导致病毒清除延迟和抗病毒药物耐药的出现。
流感增加了侵袭性曲霉病的发生风险,尤其是在免疫功能低下患者中,初期常为隐匿性感染,因此建议采用曲霉菌抗原和PCR对呼吸道分泌物进行直接监测。对于接受抗真菌治疗的患者,必须实施抗真菌治疗药物监测。
目前的数据不足以支持常规使用任何免疫治疗。尚需完善动物实验数据和开展详细的系统性临床研究,包括对优先使用的治疗方法如恢复期血浆和干扰素进行连续的病毒学检测(如病例数足够,则进行随机对照研究)。目前,由MERS-CoV所致的重症呼吸道感染患者的临床处理主要依赖于细致的强化支持治疗和并发症的预防。
四、病毒感染的宿主导向治疗
1. T细胞治疗
在造血干细胞移植患者中完成的研究显示,过继转移抗原特异性T细胞可以恢复保护性免疫,预防或逆转由机会性病毒感染如巨细胞病毒所致的疾病。将供者来源的T细胞过继转移给移植受者可以通过病毒特异性T细胞的扩增促使感染缓解,同时伴有临床状况的改善。
转移供者T细胞有发生重度急性移植物抗宿主病的风险,因此大多数T细胞治疗在淋巴细胞计数较低的患者中实施。淋巴细胞减少使得可以被转移的T细胞数量非常少,随后这些T细胞在淋巴细胞减少的宿主中增殖,如果患者在T细胞治疗期间未接受免疫抑制治疗,则上述细胞增殖很可能是IL-7和IL-15作用的结果。
针对耐药巨细胞病毒株的T细胞治疗对肺移植受者具有临床意义。T细胞扩增需要一定时间才能诱导病毒感染的缓解。在需要临床快速起效的情况下,有多种方法可能适用,如使用载有病原体相关肽的人工合成MHC抗原(所谓的MHC肽四聚体或多聚体),可使病原体特异性淋巴细胞表达病原体特异性T细胞受体。
通过使用可溶性MHC肽复合物可以分离出病原体特异性T细胞,随后立即被转移给病毒感染患者进行挽救治疗。采用多种靶向不同感染病原体的刺激物也可实现T细胞扩增。针对巨细胞病毒、EB病毒和腺病毒多种抗原的T细胞扩增可以为干细胞移植后提供广泛的抗病毒作用。
另一种与体外T细胞扩增无关的方法是确认能够识别病毒感染细胞的T细胞受体,从而转移至受者的效应细胞。经基因工程处理的T细胞还可产生能够阻断病毒感染的抗病毒RNA。
2. 反义分子
人工合成的反义分子如磷酰二胺吗啉代寡核苷酸在结构上与RNA相似,但磷酸二酯键被中性的磷酰二胺键所取代,核糖环被六元吗啉环所取代。这些分子通过抑制翻译、破坏RNA二级结构和干扰前体mRNA剪接,从而改变基因表达。磷酰二胺吗啉代寡核苷酸连同富含精氨酸的穿膜肽对细菌病原体的作用已经被反复验证,因而可以作为一个可行的方法用于任何微生物基因。
3. 特定的抗体治疗
感染病原体的特定生物治疗针对的不仅是耐药病原体,还包括其免疫逃逸机制。一种靶向CD19(B细胞标记物)的抗体被融合入T细胞信号分子后可以在T细胞中表达,一旦遇到其目标靶抗原即可杀死靶细胞。在移植后增生性疾病中,这种CD19嵌合抗原受体细胞被用于清除EB病毒阳性的淋巴瘤细胞。
为了有效清除病原体感染细胞,可以采用相似的方法,只要存在特异性很高的抗体,并且靶分子仅在感染细胞上表达。
五、耐药细菌所致的呼吸道感染
在能够导致呼吸道感染的特定细菌病原体中,抗生素耐药率和耐药谱仍在不断增加,令人担忧。对3种或以上抗生素耐药的多药耐药肺炎链球菌于1977年在南非首次发现,随后在多个国家出现,美国和西班牙的多药耐药肺炎链球菌比例高达30%-50%。欧洲抗生素耐药监测系统显示,22.2%的肺炎链球菌对青霉素中度敏感,10.9%对青霉素耐药,21.1%对红霉素耐药。
对多药耐药和泛耐药革兰阴性菌的关注主要集中在肺炎克雷伯菌、肠杆菌属(能够产生广谱β内酰胺酶、肺炎克雷伯菌碳青霉烯酶、NDM1和AmpC)、鲍曼不动杆菌和铜绿假单孢菌。在对美国健康中心的一项调查中,78%的革兰阴性菌对除粘菌素(62%的不动杆菌属、59%的假单胞菌属和52%的肠杆菌属对其耐药)以外的所有抗生素耐药。治疗这些感染可选择的药物有限。
对产广谱β内酰胺酶的病原菌建议使用碳青霉烯类药物。在一项荟萃分析中,经校正的意向治疗分析显示多尼培南治疗铜绿假单胞菌感染较对照药物更有效。多粘菌素B和粘菌素是浓度依赖性杀菌剂,可与细菌的细胞膜结合,对不动杆菌属有可靠的活性。新型β内酰胺酶抑制剂和抗生素联合治疗可能作为权宜之计以满足临床需要。
抗生素的研发线仍然较窄,全球关注的焦点集中在必须增加新型抗生素和其他抗菌新方法开发领域的投资,并且呼吁全球更谨慎地使用现有的药物。
六、多药耐药肺结核
1. 发病率
2012年,全球估计有130万人死于结核,其中17万为多药耐药结核。多药耐药结核是由至少对异烟肼和利福平耐药的结核分枝杆菌所引起,目前已在全球广泛传播,2012年估计病例数达50万。广泛耐药结核即对利福平、异烟肼和氟喹诺酮耐药,并且对3种二线注射药物(阿米卡星、卡那霉素和卷曲霉素 )中至少1种耐药,目前已有92个国家报道该病。
WHO建议对广泛耐药或多药耐药结核使用二线药物18-24个月或更长时间。无论是采用个体化方案还是标准方案,治疗成功率均较低,因而亟需开发新的药物和方案。
2. 新药研发线
过去5年中,在多药耐药和广泛耐药结核治疗领域出现了很有希望的新药研发线。通过重新开发现有药物,包括重新构造现有的抗菌化合物和重新设计支架,发现了新的化合物。两种新药delamanid(OPC-67683)和bedaquiline(TMC207或R207910)已获得管理当局的批准。这些新药可与较老的药物联合应用治疗多药耐药结核。
3. 辅助性宿主导向治疗
目前已合理开发了多种辅助性免疫治疗用于多药耐药结核。非甾体抗炎药可以降低小鼠的结核分枝杆菌载量,并减轻肺部疾病。外排泵抑制剂如维拉帕米和利血平可降低巨噬细胞诱导的药物耐受性,因而可以作为辅助性宿主导向治疗。磷酸二酯酶抑制剂如西洛他唑和西地那非可通过减轻组织炎症提高分枝杆菌清除率,并缩短杀菌时间。
涉及细胞因子或其抑制剂及其他免疫调节剂的多种辅助性免疫疗法正在接受评估,用于减轻由对抗结核分枝杆菌的炎症反应引起的损伤。各种细胞因子方案包括干扰素或IL-2已接受评估,其效果各异。大环内酯类抗生素的抗炎作用值得进一步研究。采用全基因组测序能够快速明确结核分枝杆菌的耐药模式,从而制定个体化治疗方案。
其他免疫调节策略包括在多药耐药结核患者中恢复有效的抗病原体免疫反应(从而减轻肺组织中的有害反应),同时输注患者自体骨髓来源的基质细胞。一项1期研究显示该操作是安全的,正在计划2期研究评估间充质干细胞辅助治疗对临床和微生物学结果的影响。
七、真菌性呼吸道感染
1. 发病率
全球报道的真菌性侵袭性呼吸道感染日益增加(表3)。
表3. 常见真菌性肺部感染的发病率和死亡率
曲霉病肺孢子菌肺炎
侵袭性 慢性 变应性支气管肺曲霉病
发病率(每100 000人) 8.6 10.4未知 5.6
患病率(每100 000人) .. 32.8286..
全球的疾病负担~200 000 ~3 000 000 4 800 000 ~400 000
未治疗的死亡率 ~100% ~30% <1% 100%
治疗后的死亡率 30%-90% ~10% <1% 10%-20%或50%
两种最常见的肺部真菌病原体是烟曲霉和肺孢子菌。随着感染HIV的人越来越多、肿瘤患者使用免疫调节剂不断增多、以及广谱抗生素的使用,上述病原体正日益成为欧洲、非洲和亚洲重症患者发病和死亡的主要病因。一些复发或未经微生物学确诊的多药耐药结核患者需要考虑其他诊断,包括慢性肺曲霉病,对于多药耐药结核患者,如涂片和培养阴性,则应进行更全面的检查以明确是否有真菌感染。
2. 侵袭性肺曲霉病
曲霉菌是侵袭性肺病最重要的真菌病原体,由烟曲霉所致的病例超过75%。伏立康唑是侵袭性曲霉病最有效的治疗药物,但在除南美洲以外的所有大洲均出现了耐药。由于农业中广泛使用唑类作为杀菌剂,导致泛唑类耐药的发生。耐药也可发生于治疗期间,特别是伊曲康唑,并且可能与低血药浓度和高真菌载量相关。
模型显示,超过650万人有真菌致敏的重度哮喘,多达50%的至二级医疗机构的成人哮喘患者有真菌致敏,估计有480万成人有变应性支气管肺曲霉病。对烟曲霉敏感的哮喘患者发生支气管扩张的几率较不敏感的患者明显增高。通过曲霉菌血清学检测(IgE和IgG)以及痰PCR和抗原检测对囊性纤维化患者的曲霉病进行再分类,结果发现了3种不同的曲霉病。
18%为变应性支气管肺疾病,15%为曲霉菌致敏,30%为曲霉菌性支气管炎;其余患者无疾病。长期口服抗真菌药物可使60%-80%的哮喘患者获益,但在囊性纤维化患者中未证实获益。烟曲霉耐药在整个欧洲均有报道,囊性纤维化患者样本中的检出率约为4%。
3. 播散性伊蒙菌属感染
2009年在AIDS患者中发现了一种可导致播散性感染的新型真菌。基于ITS1和ITS2测序的分子鉴定显示,该新型菌种的所有分离株与伊蒙微小菌和pasteuriana伊蒙菌非常相似,与荚膜组织胞浆菌的相关性略远。
感染的临床特征包括发热、体重减轻、贫血、类似于播散性组织胞浆菌病的皮损,以及与肺结核相似的胸部影像学表现。对来自皮肤和血液(非痰或脑脊液)的样本进行真菌培养。患者接受静脉两性霉素B序贯伊曲康唑治疗可获得明显的临床疗效。
4. 抗真菌治疗进展
一项评估伏立康唑联合阿尼芬净治疗177例侵袭性曲霉病患者的大规模研究未能达到死亡率下降的主要终点,但半乳甘露聚糖阳性患者似乎获益最大。侵袭性曲霉病治疗指南仍推荐伏立康唑优于其他所有的治疗方法,联合治疗不常规推荐。泊沙康唑片剂的生物利用度较口服混悬液更高,可一天1次给药,美国FDA已批准了该药的静脉注射混悬剂。
等待批准的唯一新药是艾沙康唑,一种广谱的唑类药物,有静脉和口服制剂(2014年7月递交审批申请)。伊曲康唑在妊娠早期应用似乎是安全的,而氟康唑可使法洛四联症的发生风险增加1-3/1000。
促使新型抗真菌药物研发的因素包括有效率不充分、缺乏棘白菌素类口服制剂、药物相互作用、重要的药物毒性反应(特别是两性霉素B和伏立康唑)及三唑类和棘白菌素类耐药。多种药物被重新开发作为抗真菌药物,新药正在研发中(表4)。
表4. 正在研发中的新型抗真菌药物

用于治疗抑郁症的舍曲林在一个小鼠隐球菌感染模型中与氟康唑有协同作用。钙调磷酸酶抑制剂和雷帕霉素靶分子抑制剂具有抗真菌活性,并且与唑类药物有协同作用。最初开发用于肿瘤治疗的Hsp90抑制剂在体外和动物模型中可提高氟康唑的活性。依诺沙星是一种氟喹诺酮类抗生素,在小鼠念珠菌病模型中显示出活性。
5. 宿主导向治疗
虽然唑类药物对侵袭性肺曲霉病的治疗很重要,但免疫抑制程度和其他免疫因素对治疗效果也有影响。异基因造血干细胞移植后,过继转移直接针对侵袭性肺真菌感染(特别是念珠菌、曲霉菌和毛霉菌感染)的病原体特异性T细胞可以改善抗真菌免疫反应。
T细胞反应为1型MHC限制性(CD8阳性T细胞)或II型MHC限制性(CD4阳性T细胞),因此有效的T细胞反应需要匹配患者的遗传背景。T细胞转移的开发是基于一个很有希望的发现,即转移病原体特异性T细胞克隆可以诱导有临床意义的反应。已有多种方法用于获得这些病原体特异性T细胞。
抗病原体特异性T细胞可以在合适的体外条件下(常借助重组细胞因子、合成肽或表达病原体的细胞成分)实现扩增。T效应细胞可以通过是否产生γ干扰素进行识别,采用干扰素捕获方法进行移除,并转移给患者。此方法扩增T细胞(来自患者自身或MHC匹配的供者)需要时间。
通过该方案能够实现对曲霉菌属、念珠菌属和毛霉菌属有活性的T细胞(通过是否产生γ干扰素识别)扩增。当再次遇到靶抗原时,T细胞增殖,并增强巨噬细胞的抗真菌活性。
八、结论
鉴于微生物群具有显著的遗传和适应能力可塑性,新的和耐药的细菌、病毒及真菌不断出现。呼吸道感染成为全球两大死亡原因之一。微生物不会尊重国际边界,便捷的旅行和空中运输使其成为全球健康的威胁。
随着抗生素耐药不断增多和治疗选择变得局限,迫切需要更多的国际间合作来共同对抗新出现的微生物和多药耐药微生物。研发新型治疗方法的同时需要制定有关抗微生物药物使用和处方的国际准则。
重要信息
呼吸道感染成为全球两大发病和死亡原因之一。耐药的细菌、病毒和真菌在全球持续出现。
多药耐药细菌、唑类耐药真菌和奥司他韦耐药甲型流感病毒H1N1所致的呼吸道感染病例数已显著增加,提示目前用于重症呼吸道感染治疗的抗生素、抗病毒药物和抗真菌药物可能较为局限。
禽流感病毒H7N9的大范围传播、禽流感病毒H10N8的散发感染和中东呼吸综合征冠状病毒感染的持续暴发凸显了开发更有效的抗病毒药物的迫切性。
研究的重点是重新开发现有抗病毒药物的一般或特殊用法,或者联合其他辅助性治疗,如免疫调节剂和宿主导向治疗。
在大多数国家,仅有一类有效的抗病毒药物获批用于流感的预防和治疗,即神经氨酸酶抑制剂(奥司他韦、帕拉米韦、扎那米韦和那尼纳米韦)。
对于泛耐药革兰阴性菌,可选择的抗生素治疗较为局限,新型抗生素的研发线仍然较窄。
需要在全球范围内增加新型抗生素和其他抗菌新方法开发领域的投资,并且更谨慎地使用现有的抗生素。
研发新型治疗方法的同时需要制定有关抗微生物药物使用和处方的国际准则。
对MERS-CoV感染可能有用的抗病毒制剂
? 中和抗体
? 恢复期血浆
? 来自转基因奶牛的多克隆人免疫球蛋白
? 马的F(ab’)2抗体片段,骆驼抗体
? 抗S单克隆抗体
? 干扰素
? α干扰素
? β干扰素
? 重新开发的药物
? 利巴韦林(联合或不联合干扰素)
? HIV蛋白酶抑制剂(洛匹那韦,奈非那韦)
? 亲环素抑制剂(环孢素,阿拉泊韦)
? 氯喹(体外有活性)
? 霉酚酸
? 硝唑尼特
? 重组人甘露糖结合凝集素
? 针对MERS-CoV关键基因的小干扰RNA(siRNA)
相关热词搜索:
上一篇:默沙东以84亿美元收购Cubist
下一篇:突变小鼠挑战遗传性状的遗传学规律
频道总排行
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(12)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)