DIAIH与AIH,是否“你”中有“我”?
2012-10-21 11:23:46 来源:37度医学网 作者:刘玉兰 评论:0 点击:
北京大学人民医院消化科成功举办了“第三届免疫介导消化系统疾病论坛”,针对临床医生关注的免疫介导消化系统疾病相关问题邀请国内外知名专家,就药物性肝损伤伴自身免疫现象和自身免疫性肝炎、肠白塞病与克罗恩病、肛瘘、免疫球蛋白(Ig)G4相关疾病、原发性胆汁性肝硬化治疗进展等话题进行了深入探讨,本报将陆续刊登相关内容,敬请关注。本期为北京大学人民医院刘玉兰教授的精彩演讲。
发生机制
药物性肝损伤机理
药物性肝损伤(DILI)根据其发病特点,主要分为肝细胞损伤、胆管系统损伤及混合性肝损伤。DILI主要通过药物代谢产物对肝脏的直接损伤 (DILI可预测部分)与免疫(过敏)特异质机制损伤(DILI不可预测部分)介导,后者常与个体差异有关,通常有发热、皮疹、关节痛和嗜酸细胞水平增高 等全身症状,并可出现自身抗体阳性。多次或长时间暴露于同一种药物,将可能引起药物诱导性自身免疫性肝炎(DIAIH)。
DIAIH产生机理
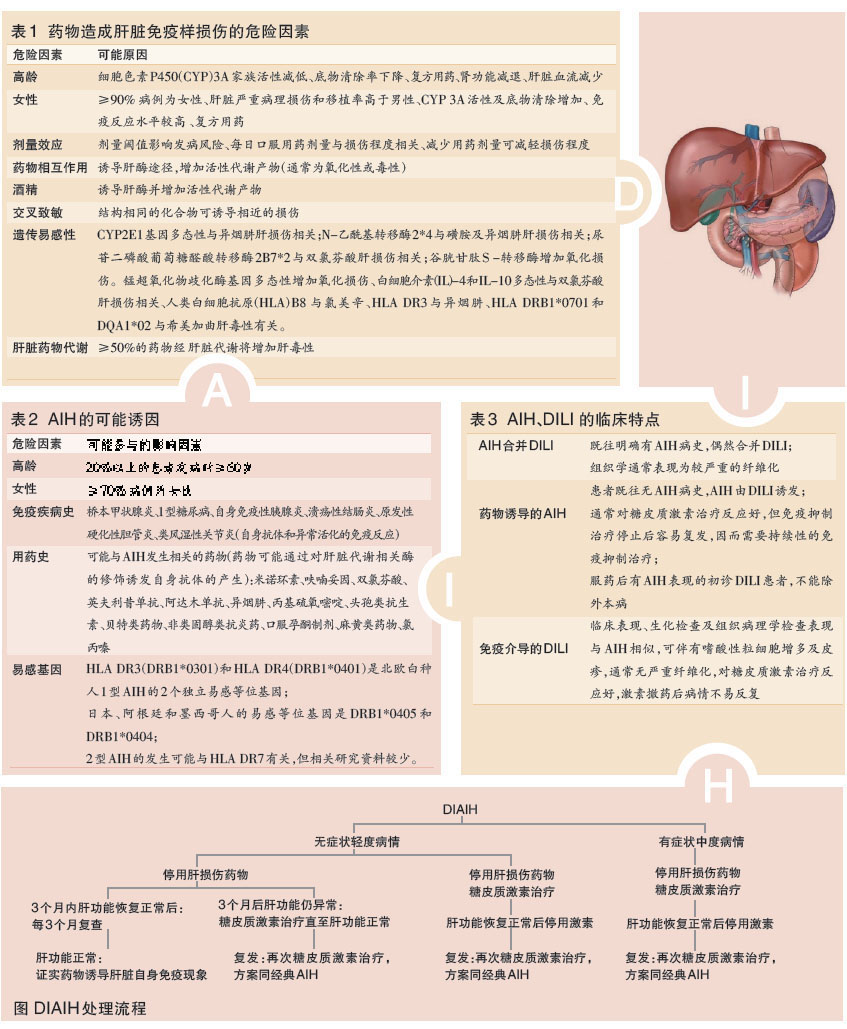
目前研究认为,与自身免疫性肝炎(AIH)类似,DIAIH同样与宿主的遗传背景、药物诱导和环境因素作用等有关,有一定基因易感性的患者服用 降脂药、抗结核药、口服激素及多种中草药在内的药物后,因肝脏细胞色素酶遗传差异造成肝脏对药物代谢能力下降;若同时或先后服用多种结构类似药物可产生交 叉反应,在造成肝脏损伤的同时诱导自身抗体产生,部分患者可能由于药物的诱发作用进一步形成AIH(表1、2)。
临床特点
两者临床特点
AIH和DILI均多发生于老年女性,症状轻;可仅表现为黄疸及转氨酶水平的异常、伴或不伴有皮疹、嗜酸性粒细胞血症及高丙种球蛋白血症;通常情况下糖皮质激素治疗有效。
DILI常在肝功能发生异常前有较明确的用药史,急性起病,伴或不伴有可检测到的自身抗体(且肝功能恢复后抗体可较长期存在),停用激素后不易复发。
AIH病程通常隐匿,自身抗体可出现在病程的各个时期,发现时往往已经有肝硬化表现或较易进展为肝硬化,停用激素后容易复发。
组织学上区分
两者的组织学表现均可为界板炎、多小叶融合坏死,门脉内淋巴细胞浸润,小叶内多种免疫细胞浸润及肝内胆管淤胆。
AIH的灶状坏死、门脉炎较常见,肝小叶内较多淋巴细胞、浆细胞、嗜酸性粒细胞浸润,纤维化发生时间早。
不论是以肝细胞损伤为主、还是伴有胆管损伤的DILI,灶状坏死和门脉炎发生较少、纤维化发生程度轻;在以胆管损伤为主的DILI中,很少出现小叶内细胞浸润。
由于AIH患者就诊时通常已服用多种药物,在此基础上还应鉴别是否存在AIH合并DILI的情况(表3)。发病机制、临床表现、实验室检查和病理特点相似,均使鉴别DILI和AIH成为临床难题。
鉴别诊断
接诊到可疑用药史患者,通常应追问其是否有长期酗酒史并检测血清学指标,除外酒精性和病毒性肝炎,但免疫学指标筛查往往不能更好地指导临床工作。AIH或DILI均可出现或不出现自身免疫指标异常,通常表现均为不明原因转氨酶水平升高。
发病机制分析 DILI药物介导或诱导的免疫损伤,在很大程度上参与了发病过程。在AIH发生过程中,部分患者使用了诱发自身免疫启动的药物。所以,DILI伴有自身免疫现象及药物诱导的AIH难以被区分。
肝脏病理学指标 依靠单次肝脏病理学指标可能不能很好区分DILI和AIH,同一份肝脏病理标本在不同病理医师、医院可能得到完全不同的诊断。有研究机构尝试采用多元参数预测方程,但该模型仍大量依赖病理学指标,有患者在病理诊断DILI后数年才表现出AIH的典型血清学及病理学特点。
诊断及鉴别 疾病初期的AIH和DILI患者服用保肝降酶药后,血清酶学指标均可明显下降;但DILI伴自 身免疫现象患者经激素治疗后常无纤维化,而AIH患者接受保肝降酶药物及激素治疗后,病情也非常容易反复并倾向于形成纤维化和硬化。因此,对有可疑用药史 及一定血清免疫学异常患者,应从临床病程、治疗效果及临床转归全面分析(图)。对疾病初期或转氨酶轻中度升高者不推荐特别积极使用降肝酶药物;对有用药史 和血清免疫学异常的转氨酶升高患者应长期随访,以免遗漏AIH诊断。(北京大学人民医院 李晶整理 刘玉兰教授审阅)
上一篇:慢性肝病患者怎么吃?
下一篇:POEM治疗贲门失弛缓症专家共识意见
频道总排行
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(12)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)